In den letzten Jahren erfolgt sowohl im ambulanten als auch im stationären Bereich eine Zunahme von Antibiotikaresistenzen. Aus diesem Grund sollte, wenn immer möglich auf Antibiotika verzichtet werden. Unkomplizierte Harnwegsinfektionen sind die ideale Voraussetzung dafür. Prof. Dr. med. Anette Kuhn, Chefarzt-Stellvertreterin der Universitätsklinik für Frauenheilkunde im Inselspital Bern, gibt einen Überblick über unterschiedliche Möglichkeiten in den verschiedenen Lebensphasen der Frau.
In vielen Fällen sind Antibiotika unabkömmlich und können Leben retten, sie bringen aber auch Risiken mit sich, die sorgfältig gegen ihren Nutzen abgewogen werden müssen. Neben allergischen Reaktionen gefährdet die Einnahme von Antibiotika auch das gesunde und normale Mikrobiom des Menschen. Das Risiko für andere Erkrankungen steigt, da die gesunde Darmflora im Verdauungstrakt bei einer Antibiotika-Therapie beeinflusst wird. Ebenso erhöht sich durch die Einnahme von Antibiotika das Risiko für Pilzinfektionen, etwa der Scheide oder von Mund und Rachen, da das natürliche Gleichgewicht zwischen Bakterien und Pilzen auf den Schleimhäuten gestört wird. Ein falscher Umgang mit Antibiotika führt darüber hinaus dazu, dass Bakterien resistent werden.
Resistenzentwicklung – Die Bakterien wehren sich!
Da Antibiotika sowohl zur Behandlung von bakteriellen Infektionskrankheiten in der Humanmedizin als auch in der Veterinärmedizin eingesetzt werden, kann es auch in der Umwelt zur weiteren Bildung und Verbreitung von antibiotikaresistenten Bakterien kommen. Mit dem Abwasser, dem Klärschlamm, der Gülle oder den Gärresten werden nicht nur antibiotikaresistente Bakterien, sondern auch Antibiotikawirkstoffe in die Umwelt entlassen, die einen Selektionsdruck auf Bakterien ausüben und damit ihre Entstehung fördern. Das bedeutet, dass der Einsatz von Antibiotika sich nicht nur auf den einzelnen Organismus und seine Bakterien auswirkt, sondern mittelbar die gesamte Population betrifft. Je mehr Antibiotika eingesetzt werden, desto mehr wird die Vermehrung und Ausbreitung von resistenten Keimen in der gesamten Population begünstigt.
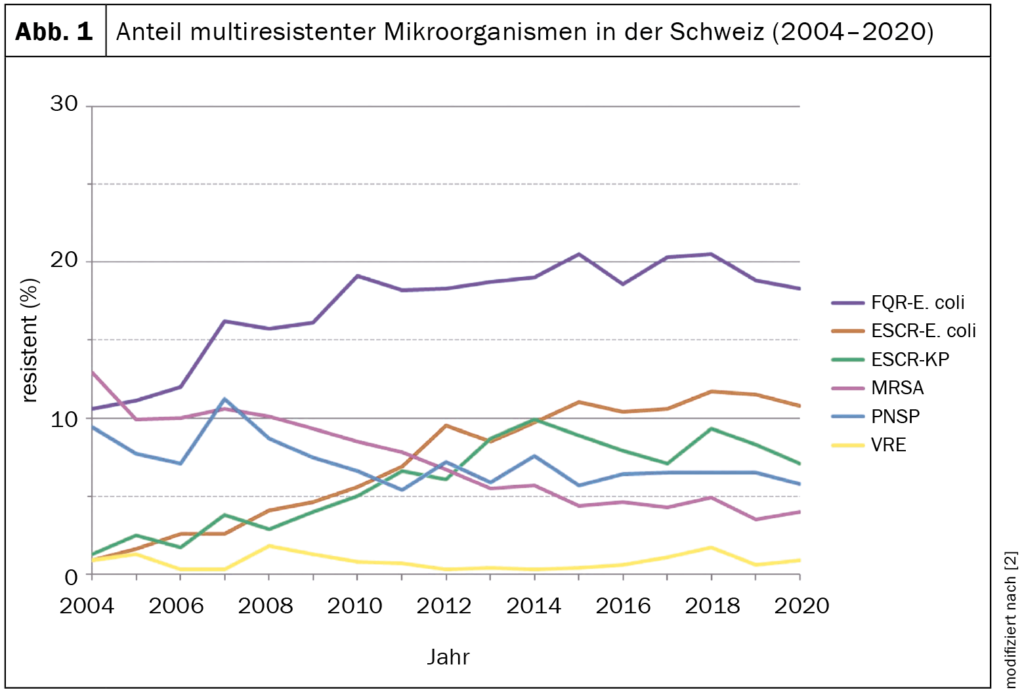
Bei einigen Bakterienarten haben Resistenzen stark zugenommen, bei anderen Arten ist die Antibiotikaresistenz stabil geblieben oder zurückgegangen. Im Fall von Escherichia coli, ein häufiger Verursacher von Blasenentzündungen, hat die Resistenz gegen Fluorchinolone zugenommen; die Resistenz gegen eine Klasse von Breitband-Antibiotika, wie Cephalosporine der dritten und vierten Generation, ebenso. Im Fall von Klebsiella pneumoniae, eine Bakterienart, die häufig die Harn- und Atemwege infiziert, hat die Resistenz bis 2014 ebenfalls deutlich zugenommen. Die Schweiz liegt bei den Resistenzen im internationalen Vergleich im Mittelfeld. Relativ zur Bevölkerungsgrösse werden hierzulande weniger Menschen von resistenten Bakterien befallen als in Frankreich, Italien oder Grossbritannien, aber mehr als in den skandinavischen Ländern und den Niederlanden. Die aktuelle Resistenzsituation in der Schweiz wird in (Abb. 1) [2] dargestellt.
Strategie zur Reduktion des Antibiotikaeinsatzes
In Europa werden pro Jahr 25.000 Todesfälle aufgrund von Resistenzen verzeichnet. Allein für E.coli treten in fünf von sechs Weltregionen mehr als 50% Resistenzen gegen Cephalosporine und Fluorchinolone auf. Nach Schätzungen der WHO werden im Jahr 2050 mehr Menschen an resistenten Keimen sterben als an Karzinomen. In der Schweiz entstand deshalb die Strategie Antibiotikaresistenzen (StAR) welche zum Ziel hat, die Wirksamkeit von Antibiotika langfristig sicherzustellen. Die vom Bundesrat verabschiedete Strategie gegen Antibiotikaresistenzen wird in den Bereichen Mensch, Tier und Umwelt umgesetzt.
Laut Prof. Dr. med. Anette Kuhn, Chefarzt-Stellvertreterin der Universitätsklinik für Frauenheilkunde im Inselspital Bern, ist daher ein angemessener Antibiotikaeinsatz bei unkomplizierten Harnwegsinfekten (HWI) angebracht. Demnach sollte stets die Überlegung erfolgen, ob bei einfachen Harnwegsinfekten ein Antibiotikum notwendig ist, oder ob alternative Substanzen zur Behandlung ausreichend sind. Auch die Prävention spielt bei Harnwegsinfekten eine entscheidende Rolle, sei es durch Überwachung, Impfungen oder Informationen über alternative Therapien. Darüber hinaus sollte ein gezielter Einsatz der Antibiotika erfolgen, die momentan noch wirksam sind [1].
Unkomplizierte vs. komplizierte und rezidivierende Harnwegsinfekte
Unkomplizierte Harnwegsinfekte zeichnen sich in der Regel durch eine normale Harnblasenentleerung und Anatomie aus. Sie werden häufig von E.Coli Keimen, Klebsiella pneumoniae oder Staphylokokken verursacht. Komplizierte Harnwegsinfekte hingegen besitzen eine strukturelle oder funktionelle Patho-Anatomie. Patienten mit dieser Diagnose neigen in der Regel zu Prädispositionen für Pyelonephritis. Nicht selten treten Restharn und rezidivierende Harnwegsinfektionen auf. Bei rezidivierenden Harnwegsinfekten erfolgen mehr als zwei Infektionen in sechs Monaten oder mehr als drei Infektionen in 12 Monaten. Für eine gezielte Behandlung sollte in diesem Fall ein Urinstatus und ein Uricult durchgeführt werden [3]. Darüber hinaus sollte bei rezidivierenden Harnwegsinfekten der Risikofaktor Stuhlinkontinenz abgeklärt werden. Sowohl bei komplizierten als auch rezidivierenden Harnwegsinfekten ist das Anlegen einer Kultur Goldstandard. Bei der Bewertung der Kultur gilt laut Europäisch Urologischer Gesellschaft 10³ bei Symptomen.
Bei männlichen Patienten gelten Harnwegsinfekte immer als kompliziert. Hier wird der Einsatz von gewebegängigen Antibiotika empfohlen, da die Infektion meist auch die männliche Adnexe betrifft. Generell gelten jedoch Frauen als Infekt anfälliger. Besonders die allgemeine urogenitale Atrophie gilt als Risikofaktor für Harnwegsinfektionen. Eine evidenzbasierte lokale Östrogenisierung kann hier allerdings Abhilfe schaffen. Evidenzbasierter Goldstandard ist die vaginale Östrogengabe. Die Anwendung von DHEA kann ebenso erfolgen, eine Testosterongabe ist hingegen mit Nebenwirkungen behaftet. Eine weitere Möglichkeit bietet darüber hinaus auch die Laserbehandlung, diese wird allerdings nicht von den Krankenkassen übernommen. Erwähnenswert ist an dieser Stelle, dass auch Patientinnen mit systemischer Östrogentherapie atrop werden können.
Therapeutische Optionen
Die interdisziplinäre S3-Leitline empfiehlt bei unkomplizierten Harnwegsinfektionen und leichten bis mittelgradige Beschwerden eine alleinige symptomatische Therapie und somit wenn möglich auf Antibiotika zu verzichten [4]. Dasselbe gilt für den Expertenbrief zu akuten und rezidivierenden Harnwegsinfekten. Hier werden zwar Antibiotika aufgeführt, diese sollten allerdings so kurz wie möglich zum Einsatz kommen. Patientinnen sollten zudem darüber informiert werden, dass die HWI in den meisten Fällen eine selbstlimitierende Erkrankung ist, dass die Symptome mit NSAR gelindert werden können und die Dauer bis zur Eradikation der Bakterien unter Antibiotika und NSAR gleich lange dauert [5]. Obwohl nach wie vor auch die post-koitale oder kontinuierliche Antibiotikaprophylaxe sehr effektiv ist, sollte diese Behandlung aufgrund von Resistenzentwicklungen vermieden werden [3].
Die Guidelines der Europäischen Urologischen Gesellschaft weisen darauf hin, dass asymptomatische Patienten nicht gescreent werden sollen, da das Screening auf asymptomatische Bakteriurie dazu führt, dass zu viele und unnötige Antibiotika verordnet werden. Unter den folgenden Bedingungen soll demnach keine asymptomatische Bakteriurie untersucht oder behandelt werden: Frauen ohne Risikofaktoren; Patienten mit gut reguliertem Diabetes mellitus; postmenopausale Frauen; ältere Patienten in Heimen; Patienten mit gestörten und/oder rekonstruierten unteren Harnwegen; Patienten mit Nierentransplantationen; Patienten vor Operationen zur Arthoplastik; Patienten mit rezidivierenden Harnwegsinfektionen. Screening und Behandlung asymptomatischer Bakteriurie erfolgt ausschliesslich vor urologischen Eingriffen, die die Schleimhaut verletzen oder bei Schwangeren mit Standard-Kurzzeitbehandlung [6].
Antibiotikafreie Alternativen
Laut einer prospektiven Kohorten Studie sind mehr als ein Drittel der Frauen mit HWI-Symptomen bereit eine Antibiotika-Behandlung zu verschieben. Die Mehrheit der Frauen mit Verzögerung berichtet sogar von einer spontanen Symptomverbesserung nach einer Woche. Es besteht zudem ein hohes Interesse an therapeutischen Alternativen [7], was sich auch in der Auswahl antibiotikafreier Alternativen widerspiegelt. An erster Stelle der therapeutischen Alternativen steht dabei keine Behandlung. Ein nicht behandelter Harnwegsinfekt klingt in der Regel nach drei bis fünf Tagen von allein wieder ab. Für die meisten Patienten ist keine Behandlung allerdings nicht zufriedenstellend. Bei leichten bis mittelgradigen Beschwerden kann auch eine alleinige symptomatische Therapie mit Antiphlogistika als Alternative zu Antibiotika erwogen werden. Hier bietet sich die Gabe von 3x400mg Ibuprofen an. Bei der Gabe von Ibuprofen ist die Entwicklung einer Pyelonephritis allerdings nicht auszuschliessen und sollte beobachtet werden [8].
Phytotherapie
Aus dem Bereich der Phytotherapie stehen der Bärentraubenblättertee sowie Extrakte aus Birke und Goldrute, wie beispielsweise die Hänseler Blasendragées, zur Verfügung. Seit März 2021 ist zudem das Präparat Canephron in der Schweiz verfügbar. Canephron ist einerseits antiphlogistisch, wirkt analgetisch und antinozizeptiv sowie spasmolytisch und antiadhäsiv. Es besteht aus Rosmarinblättern, Tausendgüldenkraut und Liebstöckelwurzel und kann in der Schwangerschaft angeboten, nicht jedoch in der Stillzeit erwogen werden, da bisher keine Daten hierzu existieren. Eine randomisierte, kontrollierte klinische Nichtunterlegenheitsstudie zeigt, dass die pflanzliche Therapie mit Canephron (BNO 1045) bei der Behandlung akuter unkomplizierter Harnwegsinfektionen nicht unterlegen ist, sondern das Potenzial hat, den ambulanten Einsatz von Antibiotika bei Harnwegsinfekten zu reduzieren. Canephron hatte einen deckungsgleichen Effekt auf die Beschwerden der Patientinnen, wie Fosfomycin-Trometamol (FT). Nach vier Tagen konnten die Beschwerden sowohl mit Canephron als auch mit Fosfomycin um die Hälfte reduziert werden [9].
Ein weiteres Präparat aus dem Bereich der Phytotherapeutika ist Angocin. Die Wirkstoffe sind Senföle aus Kapuzinerkresse und Meerrettichwurzel, welche die Vermehrung von Bakterien und Viren hemmen. In einer Kohortenstudie wurde die Wirksamkeit und Verträglichkeit von Angocin untersucht. Die Ergebnisse zeigen, dass die Therapie mit dem pflanzlichen Präparat bezüglich der Wirksamkeit mit Standard-Antibiotika vergleichbar ist. Darüber hinaus zeichnet sich Angocin in allen Indikationen durch ein deutlich geringeres Nebenwirkungspotential als die Therapie mit Standard-Antibiotika und somit durch eine bessere Verträglichkeit aus [10].
Weitere Behandlungsmöglichkeiten und Prophylaxe
Sowohl zur Prophylaxe als auch zur Therapie steht der Wirkstoff D-Mannose zur Verfügung. Der in Femannose enthaltene natürliche Einfachzucker bindet FimH-Adhesin der Fimbrien, was die E.coli Bakterien daran hindert sich an die Blasenwand zu heften. Die Behandlung ist ein bisschen aufwendiger und beinhaltet drei Sachets vom ersten bis dritten Tag und zwei Sachets am vierten und fünften Tag. Die Einnahmen sollten über den Tag verteilt erfolgen. Zur Vorbeugung sollte ein Sachet täglich über mindestens einen Monat eingenommen werden. Eine randomisierte klinische Studie hat die Wirksamkeit getestet und mit Nitrofurantoin verglichen. Das Risiko einer wiederkehrenden Harnwegsinfektion konnte bei beiden signifikant reduziert werden, bei D-Mannose besteht zudem ein signifikant geringeres Risiko für Nebenwirkungen [11].
Als Prophylaxe bieten sich darüber hinaus auch enterale und parenterale Impfungen an. Die enterale Impfung wird mit Urovaxom durchgeführt und spricht gut bei wiederkehrenden E.coli Infekten an. Die parenterale Impfung wird mit Strovac durchgeführt und sollte bei Patienten Anwendung finden, bei denen wechselnde Keime auftreten. Strovac ist in der Schweiz allerdings nicht offiziell verfügbar und muss über eine internationale Apotheke bestellt werden. Zudem wird der Impfstoff nicht von allen Krankenkassen übernommen.
Quelle:
1. Prof. Dr. med. Anette Kuhn: «Harnwegsinfektionen – muss es denn immer ein Antibiotikum sein?». Vortrag Jahreskongress gynécologie suisse 2021, 24.06.2021.
2. Bundesamt für Gesundheit: Meldungen ausgewählter multiresistenter Mikroorganismen in der Schweiz. 2020. https://www.bag.admin.ch/dam/bag/de/dokumente/mt/star/anresis/bulletin-resistenzsituation-in-der-schweiz.pdf.download.pdf/bulletin-meldungen-resistenzen-schweiz-15.11.19-de.pdf.
3. Aydin, A. et al.: Recurrent urinary tract infections in women. Int Urogynecol J 2015; doi: 10.1007/s00192-014-2569-5.
4. Interdisziplinäre S3-Leitline Unkomplizierte Harnwegsinfektionen 04/2017. AWMF-Register-Nr. 043/044.
5. Betschart, C. et al.: Akute und rezidivierende Harnwegsinfektionen. Expertenbrief No 58, 2018.
6. Bonkat (Chair), G. et al.: EAU Guidelines on Urological Infections, 2020. https://uroweb.org/wp-content/uploads/EAU-Guidelines-on-Urological-infections-2020.pdf.
7. Knottnerus, B. et al.: Women with symptoms of uncomplicated urinary tract infection are often willing to delay antibiotic treatment: a prospective cohort study. BMC Fam Pract 2013; doi: 10.1186/1471-2296-14-71.
8. Gágyor, I. et al.: Ibuprofen versus fosfomycin for uncomplicated urinary tract infection in women: randomised controlled trial. BMJ 2015; doi: 10.1136/bmj.h6544.
9. Wagenlehner, F. et al.: Non-Antibiotic Herbal Therapy (BNO 1045) versus Antibiotic Therapy (Fosfomycin Trometamol) for the Treatment of Acute Lower Uncomplicated Urinary Tract Infections in Women: A Double-Blind, Parallel-Group, Randomized, Multicentre, Non-Inferiority Phase III Trial. Urol Int 2018; doi: 10.1159/000493368.
10. Goos, K.-H. et al.: Wirksamkeit und Verträglichkeit eines pflanzlichen Arzneimittels mit Kapuzinerkressenkraut und Meerrettich bei akuter Sinusitis, akuter Bronchitis und akuter Blasenentzündung im Vergleich zu anderen Therapien unter den Bedingungen der täglichen Praxis. Arzneimittelforschung 2012; doi: 10.1055/s-0033-1351284.
11. Kranjčec, B. et al.: D-mannose powder for prophylaxis of recurrent urinary tract infections in women: a randomized clinical trial. World J Urol 2014; doi: 10.1007/s00345-013-1091-6.
Isabell Bemfert




Comments are closed.